Меднение
Шифры наносимых покрытий: М, М.бМатериал основы: углеродистые стали, нержавеющие стали, алюминиевые и титановые сплавы
Габариты изделий: до 1500х1500х1500 мм. Масса до 1 000 кг.
Нанесение покрытий на изделия любой сложности
ОТК, паспорт качества, работа в рамках ГОЗ
Общая информация
Меднение – это процесс гальванического нанесения слоя меди толщиной от 1 мкм до 300 мкм и более (в ряде случаев до 3-4 мм).
Медные покрытия обладают высоким сцеплением (адгезией) с различными металлами, высокой пластичностью и электропроводностью.
Области применения деталей с медными покрытиями зависят от того, используется ли медное покрытие как функциональное, или же медное покрытие выступает подслоем для нанесения других гальванических покрытий.
В атмосферных условиях медные покрытия легко окисляются и покрываются оксидной плёнкой, которая предохраняет их от дальнейшего разрушения.
Основные области применения медных покрытий
— для декоративных целей. В настоящее время большой популярностью используются старинные медные изделия. Гальваническое меднение позволяет наносить медные покрытия, которые после специальной обработки «состариваются», или приобретают другой требуемый внешний вид. Медное покрытие непосредственно после нанесения имеет яркий розовый цвет (блестящий или матовый, в зависимости от технологии нанесения).
— для гальванопластики. Гальваническое меднение применяется для изготовления металлических копий изделий различной формы и размеров. Создаётся восковая или пластиковая основа, которая покрывается электропроводящим лаком и слоем меди толщиной 1 — 2 мм. Такая технология меднения часто используется при изготовлении сувениров, ювелирных изделий, барельефов, волноводов и матриц.
 Благодаря низкой цене меднения, по сравнению с покрытием серебром или золотом, покрытия часто применяются при меднении электротехнических шин, контактов, электродов и других элементов, работающих под напряжением. Часто меднение используется как покрытие под пайку. Также, медные покрытия используются в узлах с высокой нагрузкой в качестве твёрдой смазки и защиты от задиров, к примеру, при свинчивании резьбовых соединений.
Благодаря низкой цене меднения, по сравнению с покрытием серебром или золотом, покрытия часто применяются при меднении электротехнических шин, контактов, электродов и других элементов, работающих под напряжением. Часто меднение используется как покрытие под пайку. Также, медные покрытия используются в узлах с высокой нагрузкой в качестве твёрдой смазки и защиты от задиров, к примеру, при свинчивании резьбовых соединений. Меднение металла часто применяется в реставрационных работах при восстановлении хромированных частей автомобильной или мото-техники, при этом наносится большой слой меди 100-250 мкм и более, который закрывает поры и дефекты металла, шлифуется и выполняет роль новой основы для нанесения последующих покрытий.
Очень простой способ меднения предметов
… Иногда это не только «красиво» но и полезно!
Идея не новая (и не моя)-заинтересовало практическое применение в быту, особенно учитывая необычную простоту процесса и доступность всех необходимых компонентов.
Начну, пожалуй, с рецепта изготовления «напитка»: компонентов минимум…
| Понадобиться обычный медный купорос, электролит (из автомагазина) и |
| 50 грамм купороса необходимо размешать в 200-250 граммах воды |
Тщательно перемешиваем и осторожно доливаем 50 грамм электролита |
Полученный раствор можно хранить в этой же бутылочке, он не разлагается и не теряет своих свойств в течении длительного времени |
░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░
Практическое применение изготовленного раствора может быть довольно разнообразным:░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░░
✅ Например, хранящиеся в сарайчике сверла/метчики/развертки со временем покрылись следами коррозии.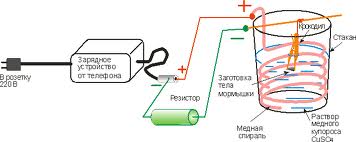
Для эксперимента возьмем пару метчиков.
легким движением руки…
получаем такой результат.
Слишком толстый слой покрытия нам не нужен, он будет хуже держаться, поэтому достаточно буквально нескольких секунд обработки.
После процедуры деталь должна высохнуть, чтобы прекратилась реакция и медь «прилипла» к стали.
| Прочность покрытия, в значительной степени, зависит от качества предварительной подготовки поверхности! |
Самый простой способ обезжиривания детали — хотя предпочтительнее использовать теплый раствор кальцинированной соды (с последующим промыванием водой) |
✅
В описанном примере, кроме защитных свойств, нанесенный слой способствует более мягкой и легкой работе с метчиком, так как трение меди со сталью в два раза ниже, чем стали со стальюИМХО описываемый способ защиты металла не самый плохой и не самый сложный-
сама обработка занимает всего несколько секунд (гораздо больше времени потребуется на очистку и обезжиривание).
✅ Металл, кстати, не обязательно окунать в раствор, можно намочить тупфер и им протирать выбранные участки или даже поупражняться в каллиграфии-наносить надписи на металлические поверхности.
✅
Поскольку, при обработке, слой меди оседает равномерно со всех сторон, понравилась идея восстановления прослабленных посадочных мест валов — ведь при подобном «напылении» ось вращения не уходит, а процесс довольно простой и дешевый, не требующий станков и сложных приспособлений
Для эксперимента отшлифовал поверхность вала, чтобы подшипник на нем болтался
«поврежденное» место многократно опускаю в раствор, до получения желаемой толщины слоя.
При необходимости, лаком/краской можно защитить поверхность или резьбу, на которой слой меди нам не нужен.
После нескольких окунаний в раствор подшипник уже рукой не натягивается — необходимо впрессовывать.
✅
Еще один вариант использования раствора — для декоративной обработки поверхностей.Макнул пару деталек для пробы. Даже без дополнительной обработки поверхности, выглядит довольно интересно
Пробовал царапать металл- покрытие получается относительно прочное…
✅
Далее… заинтересовала возможность нанесения меди на алюминий и другие металлы.
Захотелось, например, припаять алюминиевую проволоку к болту…
… и это в принципе получилось 🙂
| Есть правда нюанс- для нанесения меди на алюминий (и некоторые другие металлы) понадобится небольшая доработка нашей «гальвано-установки». |
На самом деле, емкость с электролитом и заготовкой уже является «батарейкой». При внесении второго электрода в электролит мы видим наличие электрического тока. |
Для работы с алюминием (а так же усиления и ускорения процесса), необходим дополнительный источник питания и медный электрод, для поддержания нужной концентрации меди в растворе. |
Доработанная гальвано-установка, в принципе, работает даже от «повербанки» (проверял) или маломощной зарядки от телефона, но для контроля процесса все же удобнее использовать регулируемый источник тока (при слишком больших токах наносимый слой получается относительно рыхлый, при слишком малых процесс идет крайне медленно, или останавливается).
В зависимости от размеров поверхности, я устанавливал 300-500мА, возможно потребуется подобрать оптимальные значения под конкретную заготовку.
✅
Любопытно, что нанесение покрытия возможно не только на металлы, но и на дерево, засушенные растения, насекомых и прочие неметаллические поверхности.
Подобная возможность просто находка для любителей изготовления различных декоративных предметов.
Технология нанесения не сильно отличается от описанной, просто сначала на поверхность наносится электропроводный лак или графитовый порошок, затем все по описанному выше сценарию. Понадобится некоторая сноровка и (возможно) дополнительные присадки, для получения матового или зеркального покрытия и получения необычных эффектов на поверхности (патинирование и другие).
-Варианты применения меднения не ограничиваются перечисленными выше, а главный плюс описанной технологии: простота, доступность компонентов и их мизерная стоимость.
Вероятно, описанным методом, при необходимости, можно экранировать небольшой корпус устройства (на манер корпуса ноутбука), металлизировать поверхность, в некоторых случаях восстановить или добавить дорожку на плате, сделать надпись, покрыть ручку аппаратуры в стиле стимпанкМожно покрыть медью кусок свинца и сдать в металлолом :)))и т.п…
Кстати, подобным же образом делают копии отдельных предметов (например редкой монеты) :).
По изготовлению декоративных предметов гальванопластикой тема довольно обширная, и если она интересна моим читателям, опубликую продолжение с подробностями — «историю одного эксперимента :)»
(для одного обзора слишком большой объем информации и картинок.)
На этом пожалуй и все 😉 Надеюсь идея статьи Вам понравилась.
Всем удачи и хорошего настроения!☕
Свойства и область применения медных покрытий | Меднение
Медные покрытия не рекомендуются для защиты железа и стали от коррозии. Омедненные изделия могут быть защищены от атмосферной коррозии лишь! в том случае, когда медные покрытия совершенно свободны от пор даже микроскопических размеров. При наличии пор изделия не только не будут защищены от коррозии, но, напротив, в присутствии корродирующего агента, между железом и медью начнет работать коротко замкнутый гальванический элемент, в котором железо будет играть роль анода и его коррозия будет протекать более интенсивно, чем неомедненного железа.
При наличии пор изделия не только не будут защищены от коррозии, но, напротив, в присутствии корродирующего агента, между железом и медью начнет работать коротко замкнутый гальванический элемент, в котором железо будет играть роль анода и его коррозия будет протекать более интенсивно, чем неомедненного железа.
Медные покрытия не могут также рассматриваться как защитно-декоративные. Хотя химическая стойкость меди больше, чем железа, но в наружной атмосфере с небольшой относительной влажностью медные покрытия тускнеют в результате окисления, которое протекает по параболическому закону. При повышенной влажности в порах медных покрытий происходит ржавление стали (анода). На беспористых медных покрытиях в наружной атмосфере с повышенной влажностью постепенно образуется зеленая патина, которая, по некоторым данным, представляет собой основной сульфат меди CuSO43Cu(OH)2; на морском побережье может образоваться основной хлорид меди. Устойчивость патины в различной атмосфере, по-видимому, объясняется образованием закиси меди. При анодном окислении в соответствующих электролитах можно искусственно получать патину.
Довольно широко распространен процесс меднения участков стальных деталей, подлежащих обработке резанием после термической обработки — цементации. Стальные детали иногда подвергают меднению с последующим химическим или электрохимическим окрашиванием в различные цвета. Однако наиболее широко медные покрытия используют в качестве промежуточных слоев при защитно-декоративном хромировании стальных и цинковых деталей. Широкое применение электролитических осадков меди в качестве промежуточных слоев при нанесении различных гальванических покрытий в известной мере определяется хорошим сцеплением электроосажденной меди с различными металлами. В отличие от горячих методов нанесения металлических покрытий, при которых между основным металлом и покрытием образуется промежуточный диффузионный слой, при электролитическом осаждении меди на сталь не удается обнаружить промежуточный диффузионный слой. Решающую роль для обеспечения прочного сцепления в данном случае играет тщательная подготовка поверхности основного металла — обезжиривание и травление, причем в случае химического или электрохимического удаления деформированного слоя часто наблюдается продолжение структуры основного металла в электроосажденном металле. Прочность сцепления между основным металлом и покрытием при этом приближается по величине к прочности связи между отдельными атомами в твердом металле.
Решающую роль для обеспечения прочного сцепления в данном случае играет тщательная подготовка поверхности основного металла — обезжиривание и травление, причем в случае химического или электрохимического удаления деформированного слоя часто наблюдается продолжение структуры основного металла в электроосажденном металле. Прочность сцепления между основным металлом и покрытием при этом приближается по величине к прочности связи между отдельными атомами в твердом металле.
Продолжение микроструктуры основного металла в электролитическом осадке, по-видимому, обеспечивается в тех случаях, когда основной металл имеет относительно крупнокристаллическую структуру и электролиз протекает при условиях, соответствующих образованию кристаллов примерно таких же размеров. При включении посторонних ионов, атомов или молекул осадки получаются мелкокристаллическими и продолжения структуры основного металла не наблюдается (рис. 82).
Рис. 82. Продолжение структуры основного металла электроосажденной меди (снизу вверх): серебра (а), никеля (б) (нет продолжения), в — катаной меди
При защитно-декоративном хромировании стальных и цинковых деталей роль медного слоя сводится к максимальной экономии стратегического никеля при сохранении защитных свойств суммарных покрытий (Cu+Ni+Cr) и снижению трудоемкости операций механической подготовки поверхности стальных деталей.
Как известно, медь значительно пластичнее стали и в процессе ее полировки удается получать гладкую, блестящую поверхность, на которую легко наносить блестящие никелевые покрытия. Здесь необходимо оговорить, что в последнее время достигнуты большие успехи в получении блестящих покрытий, не требующих полировки, но эта задача решена еще не полностью. При нанесении относительно тонких слоев из цианистых или пирофосфатных электролитов на стальные или цинковые детали удается получать блестящие или полублестящие медные покрытия, поверх которых после промывки можно наносить блестящие никелевые покрытия.
1.1 Медные покрытия
Медь – один из самых распространённых металлов в гальванотехнике. Медное покрытие мягкое, красноватого цвета, довольно пластичное, хорошо поддается пайке. Кроме того, медь – прекрасный проводник электричества. Тем не менее, для окончательных покрытий медь используется редко, так как быстро окисляется под действием кислорода воздуха и как следствие – тускнеет.
Превосходные выравнивающие и кроющие свойства меди делают ее идеальной для использования в качестве подложки перед нанесением других металлов. Помимо этого, благодаря своей мягкости и пластичности, медь легко полируется до яркого блеска, что позволяет получать на ней такой же яркий и блестящий слой другого металла.
Медь способна заполнять остроугольные углубления и сглаживать нежелательные неровности поверхности, позволяя наносить основной металл гладким равномерным слоем. Выравнивающие и кроющие свойства меди дают возможность избежать образования пор и пузырьков на конечном покрытии.
В качестве металлической подложки медь может наноситься на алюминий, который из-за наличия окисной пленки практически не удерживает покрытия других металлов, осаждаемых электролитическим способом. Медь – единственный металл, который можно осаждать на поверхность изделий из цинка, свинца, медно-свинцовых и цинковых сплавов, отлитых под давлением.
Меднение в кислых электролитах.
В кислых электролитах медь присутствует в виде двухвалентных ионов. Чаще всего используются сульфатные и фторборатные электролиты так как они устойчивы в эксплуатации и не токсичны, имеют высокий выход по току (95-100%) и высокую скорость осаждения. Электролиты обладают хорошей выравнивающей способностью, особенно в присутствии органических добавок – производных пиридина, гидразина, некоторых красителей.
При использовании кислых электролитов не удается получить прочно сцепленных медных осадков непосредственно на стальных изделиях из-за контактного выделения меди. Однако при введении в такие электролиты органических добавок, тормозящих процесс контактного обмена, можно получить осадки, прочно сцепленные со сталью. В промышленности перед меднением стальных изделий в кислых электролитах на них наносят подслой никеля толщиной 0,3 — 0,5 мкм.
Однако при введении в такие электролиты органических добавок, тормозящих процесс контактного обмена, можно получить осадки, прочно сцепленные со сталью. В промышленности перед меднением стальных изделий в кислых электролитах на них наносят подслой никеля толщиной 0,3 — 0,5 мкм.
Состав сульфатных электролитов и режим осаждения:
| Состав электролита (г/л) и режим осаждения |
Электролит №1 | Электролит №2 | Электролит №3 |
| Сульфат меди | 200-250 | 200-250 | 180-250 |
| Хлорид натрия | — | 0,06-0,09 | — |
| Серная кислота | 50-70 | 40-60 | 30-50 |
| Соляная кислота | — | — | 0,01-0,02 |
| Блокообразующая добавка | — | Зависит от добавки. | — |
| Температура, 0С | 18-25 | 18-25 | 18-25 |
| Катодная плотность тока, А/дм2 | 1-2 | 3-5 | 2-3 |
| Состав электролита, г/л | Электролти №4 | Электролит №5 |
| Фторборат меди | 35-40 | 220-250 |
| Кислота борфтористоводородная свободная | 15-18 | 2-3 |
| Кислота борная | 15-20 | 15-16 |
| Температура, 0С | 18-25 | 60 |
| Катодная плотность тока, А/дм2 | До 10 | До 30 |
Электролит №1 – стандартный сернокислый, при перемешивании сжатым воздухом или механическим способом катодную плотность тока можно поднять до 6-8 А/дм2. Качество и мелкозернистость осадков, получаемых из этого электролита, повышаются при введении 7-10 мл/л этилового спирта.
Качество и мелкозернистость осадков, получаемых из этого электролита, повышаются при введении 7-10 мл/л этилового спирта.
Электролит №2 – используется для осаждения блестящих медных покрытий, обладает выравнивающим действием, требует высокой чистоты компонентов.
Электролит №3 – применяется для осаждения блестящих покрытий на детали несложной конфигурации.
Электролиты №4, 5 – фторборатные, используются для осаждения толстых слоев меди. Перемешивание, как правило, производят сжатым воздухом или механической мешалкой.
Меднение в щелочных электролитах.
Составы цианидных электролитов и режимы осаждения:
| Состав электролита (г/л) и режим работы |
Электролит №1 | Электролит №2 | Электролит №3 | Электролит №4 |
| Цианид меди | 40-50 | 25-30 | 25-30 | 100-120 |
| Цианид натрия | 45-55 | 55-70 | 35-40 | 135 |
| Карбонат натрия | 10-15 | — | 20-30 | — |
| Едкий натр | 3-5 | 4-5 | До pH = 12,5 | 25-30 |
| Тартрат калий-натрия | — | — | 45-50 | — |
| Роданид натрия | — | — | — | 15-20 |
| Температура, 0С | 40-45 | 18-25 | 55-70 | 70-80 |
| Катодная плотность тока, А/дм2 | До 1,5 | 0,3-0,6 | 1,5-6,0 | 1,0-4,0 |
Электролит № 1 – один из самых распространенных в промышленности.
Электролит № 2 – применяется для предварительного меднения стальных изделий.
Электролиты № 3,4 – высокопроизводительные цианистые электролиты меднения.
Во всех цианистых электролитах отношение анодной поверхности к катодной рекомендуется поддерживать равным 2:1. Применение реверсивного тока при использовании цианистых электролитов приводит к увеличению блеска и понижению пористости покрытий.
Основное достоинство цианистых электролитов меднения – высокая рассеивающая способность, мелкозернистость осадков и возможность непосредственно осаждать медь на стальные изделия. Главные недостатки – токсичность, невысокая устойчивость, низкий выход по току, малая скорость осаждения.
Из нецианистых щелочных электролитов меднения наибольшее распространение получили пирофосфатные электролиты.
Составы пирофосфатных электролитов и режимы работы:
| Состав электролита (г/л) и режим работы |
Электролит №1 | Электролит №2 | Электролит №3 | Электролит №4 |
| Сульфат меди | 30-50 | 80-90 | 1.0-2.5 | 45-55 |
| Пирофосфат натрия | 120-180 | — | — | 200-240 |
| Гидрофосфат натрия | 70-100 | — | — | — |
| Пирофосфат калия | — | 350-370 | 80-120 | — |
| Нитрат аммония | — | 20-25 | — | — |
| pH | 7,5-8,9 | 8,5 | — | 7-8 |
| Температура, 0С | 20-30 | 50-55 | 18-25 | 55-65 |
| Катодная плотность тока, А/дм2 | 0,3-0,4 | 0,5 | 1-3 | 0,3-0,8 |
Электролит № 1 – наиболее часто применяемый в промышленности, требует при работе отношения катодной площади к анодной, равного 1:3. При нанесении покрытий на сталь, детали следует опускать в электролит под током, кроме того, в начале электролиза следует дать «толчок тока» в течении 20-50 секунд.
При нанесении покрытий на сталь, детали следует опускать в электролит под током, кроме того, в начале электролиза следует дать «толчок тока» в течении 20-50 секунд.
Электролит № 2 – применяется для меднения стали и цинковых сплавов.
Электролит № 3 – применяется для предварительного меднения алюминиевых сплавов.
Электролит № 4 – применяется для непосредственного меднения алюминиевых сплавов.
По рассеивающей способности пирофосфатные электролиты не уступают цианистым. Микротвердость и внутренние напряжения осадков, полученных в этих электролитах, существенно не отличаются от тех, что получены в цианистых.
Недостатки пирофосфатных электролитов – неустойчивость и недостаточная адгезия получаемых из них покрытий со сталью. Чаще всего применяются для нанесения меди на алюминиевые сплавы, а также при металлизации диэлектриков.
Технология и механизм гальванического меднения металла электролизом.
Содержание:
1. Что такое медь?
2. Кинетика процесса гальванического меднения.
1. Что такое медь?
Медь — металл розового цвета с атомной массой 63,5, плотностью 8,9 г/см3, температурой плавления 10830С, удельным электросопротивлением 0,017*Ом*мм. Медь пластична, твердость медных покрытий 2500-3000 МПа.
Медь интенсивно растворяется в аэрированных аммиачных и цианидных растворах, азотной кислоте, медленнее — в хромовой, слабо — в серной и почти не взаимодействует с соляной кислотой. На воздухе медь легко реагирует с влагой, углекислыми и сернистыми соединениями, окисляется и темнеет.
Стандартный потенциал меди по отношению к ее одновалентным нонам +0,52 В, двухвалентным ионам +0,34 В.
В жестких условиях эксплуатации медь и ее сплавы не должны контактировать с хромом, оловом, сталями, цинком, кадмием, алюминием и магнием.
Медные покрытия широко применяются в основном в качестве подслоя при нанесении многослойных покрытиях, а также для улучшения пайки, создания электропроводных слоёв, местной защиты стальных деталей при цементации..jpg)
2. Кинетика процесса гальванического меднения.
Для электролитического осаждения меди разработано большое количество электролитов, которые, обычно, разделяют на две группы: кислые и щелочные. Существуют как простейшие, так и достаточно сложные композиции.
Катодные поляризационные кривые для некоторых из них приведены на рисунке 1.
Рисунок 1 — Катодные поляризационные кривые при меднении из электролитов: 1 — сульфатный; 2 — пирофосфатный; 3 — цианидный ; 4 -цианидный с повышенным содержанием свободных цианидов.
2.1 Процессы в кислых электролитах меднения.
К кислым электролитам относятся сульфатные и фторборатные электролиты. Их основные достоинства — простота состава и устойчивость в эксплуатации, но они обладают низкой рассеивающей способностью. Также из них невозможно непосредственно меднить сталь из-за выпадения контактной меди, а, следовательно, плохое сцепление со сталью слоя меди. Вследствие этого меднение осуществляется после предварительного осаждения медного слоя (3-4 мкм) из щелочных электролитов или после осаждения никелевого слоя (3-5 мкм).
Из кислых электролитов наиболее распространен сульфатный электролит. Основными компонентами сульфатных электролитов являются сульфат меди и серная кислота. Электропроводность нейтральных растворов сульфата меди невелика, поэтому в них добавляют серную кислоту, которая значительно повышает электропроводность растворов температуры перемешивания.
Предполагается, что на катоде разряд двухвалентных ионов меди протекает в две стадии:
Cu2++ e → Cu+
Cu+ + e → Cu
Замедленной стадией является первая реакция. Доля каждой стадии в общей кинетике меднения зависит от состава электролита и режима электролиза: плотности тока, температуры, перемешивания.
Выход меди по току около 100 %, так как выделения водорода на катоде не происходит, поскольку потенциалы выделения меди имеют более положительные значения, чем потенциалы выделения водорода.
Повышение кислотности электролита способствует уменьшению растворимости сульфата меди, что приводит к снижению верхнего предела допустимой плотности тока. Для увеличения концентрации ионов меди в катодном слое применяют перемешивание. В этом случае кислотность электролитов можно увеличивать. Чем интенсивнее перемешивание, тем выше может быть содержание серной кислоты. Повышение температуры способствует увеличению растворимости сульфата меди: при 25 °С — 23,05 г CuSO4 на 100 г воды; при 100 °С — 73,6 г. Повышенная кислотность способствует получению более мелкокристаллических осадков.
Вблизи анодов наряду с ионами Cu2+ в растворе могут находиться в незначительном количестве ионы одновалентной меди, образующиеся в результате протекания реакции:
Cu + Cu2+↔ 2Cu+
При накоплении в растворе ионов Cu+ равновесие будет сдвигаться влево, и металлическая медь будет выпадать в виде осадка.
При недостаточной кислотности раствора сульфат одновалентной меди будет гидролизоваться с образованием Сu(ОН)2 или СuО2
Cu2SO4 + H2O ↔ Cu2O + H2SO4
В результате в электролите будут взвешенные частицы металлической меди и оксида меди, которые, включаясь в катодный осадок, делают его темным, шероховатым, а иногда — рыхлым.
Присутствие серной кислоты способствует протеканию реакций окисления одновалентной меди:
Cu2SO4 + H2SO4 + 1/2О2→ 2CuSO4 + Н2О
Cu2O + 2H2SO4 + 1/2O2→ 2CuSO4 + 2H2O
Таким образом, серная кислота прежде всего нужна для предупреждения накопления ионов Cu+ и гидролиза ее солей.
В сульфатные электролиты иногда вводят поверхностно-активные вещества. Эти вещества вводят для повышения катодной поляризации, что способствует получению более мелкозернистых плотных, иногда блестящих, осадков. Благоприятное действие этих добавок сказывается в том, что они предупреждают образование наростов на краях и выступающих частях деталей. Наилучшими добавками являются декстрин (не более 1 г/л) и фенол или его сульфосоединения (1-10 г/л).
Для получения блестящих медных покрытий предложено большое количество блескообразующих добавок, обеспечивающих зеркальный блеск покрытий, придающих им пластичность и снижающих внутренние напряжения.
При работе с электролитами для получения блестящих покрытий особое внимание следует уделять анодам. Анодный процесс растворения меди достаточно сложен и подробно описан в статье.
Взвешенные частицы шлама обычно являются причиной грубого шероховатого осадка. Вообще, медное покрытие особенно склонно к дендритообразованию при осаждении с нарушением технологического процесса, к которому относится и присутствие шлама в растворе. Частички шлама становятся при этом центрами кристаллизации и ток, вместо того, чтобы идти на зарождение новых зерен меди, расходуется на обрастание и разрастание этих частиц. Дендриты могут появляться и по другим причинам, одной из которых также является превышение допустимой плотности тока на выступающих частях деталей. Примеры дендритов на медном покрытии приведены на рисунке 2. Пример дендрита на циллиндрическом катоде и поперечный рез такого дендрита приведены на рисунке 3.
Рисунок 2 — Примеры дендритов на медном покрытии.
Рисунок 3 — Пример дендрита на циллиндрическом катоде и поперечный рез такого дендрита.
На качество получаемых блестящих покрытий большое влияние оказывает концентрация ионов Сl—. При пониженной концентрации снижается блеск покрытий и образуются прижоги на острых кромках деталей, при повышенном содержании образуются полосы на покрытиях.
Вредными примесями в медных сульфатных электролитах являются мышьяк, сурьма, некоторые органические вещества, образующие коллоидные растворы, анодный шлам.
Кроме сульфатных, используют фторборатные электролиты. Эти электролиты обладают высокой устойчивостью; получающиеся покрытия плотные и мелкокристаллические, рассеивающая способность электролитов примерно такая же, как у сульфатных. Большая растворимость фторбората меди позволяет применять повышенные плотности тока. Из этих электролитов осаждать медь непосредственно на стальные детали нельзя; необходим подслой никеля или меди из цианидных электролитов.
2.2 Процессы в щелочных электролитах меднения.
К щелочным электролитам относятся цианидные, пирофосфатные и этилендиаминовые электролиты. Основные достоинства: высокая рассеивающая способность, получение мелкокристаллических осадков, возможность непосредственно меднить стальные детали.
2.2.1 Цианистое меднение.
Довольно распространены цианидные электролиты. Условия осаждения меди из цианидных электролитов существенно отличаются от условий осаждения в кислых электролитах.
В цианидных электролитах медь находится в составе комплексных ионов, степень диссоциации, а, следовательно, и активность ионов меди очень мала. Поэтому потенциал выделения меди в них примерно на 0,9-1,2 В отрицательнее, чем в сульфатных растворах.
При малом количестве цианида аноды пассивируются. При недостаточном количестве свободного цианида, когда происходит пассивация анодов и на них разряжаются ионы ОН— с выделением кислорода, то не весь образующийся кислород выделяется в виде газа, а часть его расходуется на окисление цианида в цианит. Уменьшение содержания цианидов происходит также из-за взаимодействия их с углекислотой воздуха и образования карбонатов (NaCN → Na2CO3 ).
Содержание свободного цианида оказывает на катодный и анодный процессы противоположное влияние: для катодного процесса требуется минимальное содержание цианидов, для анодного — максимальное. При недостатке свободного KCN на анодах образуется зеленоватая пленка CuCN из-за того, что ионы меди не в состоянии перейти в комплексное соединение. Свободная поверхность анода уменьшается, плотность тока растет, и анодное растворение происходит с образованием ионов двухвалентной меди, которые в виде нерастворимого гидрата осаждаются на аноде. При этом аноды пассивируются и наблюдается интенсивное выделение кислорода.
При недостатке свободного KCN на анодах образуется зеленоватая пленка CuCN из-за того, что ионы меди не в состоянии перейти в комплексное соединение. Свободная поверхность анода уменьшается, плотность тока растет, и анодное растворение происходит с образованием ионов двухвалентной меди, которые в виде нерастворимого гидрата осаждаются на аноде. При этом аноды пассивируются и наблюдается интенсивное выделение кислорода.
Основными компонентами медных цианидных электролитов являются комплексный цианид меди и свободный цианид натрия. Из приведенных данных видно, что степень диссоциации комплексных ионов очень мала и уменьшается с увеличением содержания CN— в комплексе. Этим, по-видимому, объясняется повышение катодной поляризации при увеличении содержания свободного цианида в электролите.
Содержание меди в электролите во время работы обычно уменьшается вследствие недостаточной растворимости анодов. Снижение концентрации ионов меди в электролитах приводит к образованию пористых осадков. Кроме того, работая с малоконцентрированными медными электролитами, можно применять только пониженные плотности тока.
Постоянным компонентом цианидных электролитов является карбонат. Он накапливается в результате окисления цианида кислородом воздуха, особенно при нагревании:
2NaCN + 2Н2О + 2NaOH + О2 = 2Na2CO3 + 2NH3
Присутствие карбонатов в небольших количествах полезно, поскольку при этом повышается электропроводность электролитов. Однако при их накоплении свыше 70 г/л, а в концентрированных — до 140 г/л аноды проявляют склонность к пассивированию, а покрытия получаются пористыми. Карбонаты можно удалять при помощи хлорида бария и вымораживанием, охлаждая электролит до -5 °С. Следует отметить, что карбонаты натрия легче выпадают в осадок, чем калиевые. Сульфаты существенного влияния на процесс электролиза не оказывают.
Введение в электролит депассиваторов, в качестве которых применяют сегнетову соль KNaC4H4O6•4H2O и роданид калия KCNS, позволяет повысить рабочую плотность тока и устранить пассивацию анодов, но при этом следует одновременно повышать температуру электролита.
Высококонцентрированные по меди электролиты, содержащие депассиваторы, позволяют применять высокие плотности тока (до 10 А/дм2) при повышенной температуре и перемешивании. При этом возможно получить выход по току, близкий к 100 %.
Сульфиды, вводимые в электролит, играют роль восстановителя, предупреждая накопление в ванне ионов меди Cu2+.
Для замены ядовитых цианидных электролитов применяют пирофосфатные и этилендиаминовые электролиты.
2.2.2 Пирофосфатное меднение.
Из пирофосфатных электролитов получают медные осадки с мелкозернистой структурой. При нанесении тонких слоев осадки получаются гладкими, блестящими или полублестящими. Преимущества пирофосфатных электролитов перед кислыми заключаются в высокой рассеивающей способности и возможности непосредственно проводить меднение стальных деталей в разбавленном пирофосфатном электролите.
Основные компоненты пирофосфатных электролитов: CuSO4 или Сu2Р2О7 и К4Р2О7 или Na4P2O7. В растворах в присутствии Na4P2O7 образуется комплексная соль Na6[Cu(P2O7)2]; при избытке свободного пирофосфата может образовываться Na2[Cu(P2O7)2]. Константы нестойкости комплексов [Сu(Р2О7)2]6- и [Сu(Р2О7)2]2- соответственно равны 3•10-3 и 2•10-9.
В щелочных растворах при рН 8 и достаточном избытке свободных ионов Р2О74- медь находится преимущественно в виде шестизарядных комплексных ионов [Сu(Р2О7)2]6-.
В пирофосфатные электролиты вводят NH4NO3, который способствует повышению допустимой катодной и анодной плотностей тока и улучшает качество осадков. Из пирофосфатных электролитов можно получать блестящие осадки. В качестве блескообразующих добавок вводят Na2SeO3 совместно с лимонной или триоксиглутаровой кислотой, 2-меркаптотиазол и другие вещества.
При повышенных плотностях тока может происходить пассивация анодов за счет образования на их поверхности труднорастворимой оксидной или солевой пленки.
Катодный потенциал меди в пирофосфатных электролитах имеет более отрицательное значение, чем в кислых. Большая катодная поляризация объясняется пассивированием поверхности катода вследствие адсорбции ионов Р2О74- или образования оксидных (Сu2О8) и труднорастворимых соединений (Сu2Р2О7) в виде фазовой пленки.
Предполагают, что выделение меди на катоде из пирофосфатных растворов происходит в результате восстановления двухзарядных комплексов:
CuP2O72- + 2e—→ Cu + Р2О74-,
образующихся при диссоциации шестизарядных комплексов:
Cu(P2O7)26-↔ CuP2O72- + Р2О74-.
С повышением температуры ускоряется выделение меди, что связано как с ускорением диффузии комплексных анионов к катоду, так и с облегчением их разряда.
Структура осадков меди из пирофосфатного электролита более мелкая, по сравнению с сернокислымирастворами, с ростом плотности тока она укрупняется (рисунок 4)
Рисунок 4 — Микроизображения медного покрытия из пирофосфатного электролита при плотности тока 0,5 А/дм2 (слева) и 1 А/дм2 (справа).
Анодный выход по току в этих электролитах несколько выше катодного, поэтому при корректировке нет необходимости добавлять медные соли. Анодную плотность тока рекомендуется поддерживать в пределах 2-4 А/дм2. При более низкой плотности тока растворение идет недостаточно быстро, при более высокой — на поверхности анодов образуется труднорастворимая оксидная пленка.
Для предотвращения пассивации анодов должно быть достаточное количество свободных анионов Р2О74- и достаточно высокое рН раствора. Повышение температуры способствует отводу продуктов реакции и, следовательно, уменьшению пассивации анодов. Для этой же цели в электролиты вводят депассиваторы, которые способствуют снижению активности ионов Cu2+ в прианодном слое.
При работе пирофосфатных ванн рекомендуется проводить фильтрацию электролита: для полублестящих осадков — периодически или непрерывно, для блестящих — непрерывно.
Особенностью этилендиаминовых электролитов меднения является возможность непосредственного меднения стальных деталей. Детали в ванну загружают под током плотностью в 3-5 раз превышающей рабочую.
Данная статья является интеллектуальной собственностью ООО «НПП Электрохимия» Любое копирование без прямой ссылки на сайт www.zctc.ru преследуется по закону. Текст статьи обработан сервисом Яндекс «Оригинальные тексты»
Гальваническое покрытие медью в домашних условиях: стали, свинца, латуни
Основной задачей гальванического покрытия медью в домашних условиях или по-другому меднения является подготовка поверхности металла к его дальнейшей обработке. Такой операции могут подвергаться различные металлы, и не металлы, среди которых следует выделить:- сталь,
- латунь,
- никель и другие.
Использование меди
Благодаря своим многочисленным преимуществам данный металл получил широкое распространение. На сегодняшний день медь и ее многочисленные сплавы широко используются в промышленности. Металл актуальный для авиастроения, автомобилестроения, приборостроения и других отраслей. Не меньшей популярностью металл и изделия из него пользуются и в бытовой сфере. Меднение само по себе является одним из лучших способов покрытия тонким слоем металлической поверхности. В домашних условиях меднение можно выполнить нескольким способами.
На сегодняшний день медь и ее многочисленные сплавы широко используются в промышленности. Металл актуальный для авиастроения, автомобилестроения, приборостроения и других отраслей. Не меньшей популярностью металл и изделия из него пользуются и в бытовой сфере. Меднение само по себе является одним из лучших способов покрытия тонким слоем металлической поверхности. В домашних условиях меднение можно выполнить нескольким способами.
Гальваническое меднение в домашних условиях
Для этого понадобится:
- Медный купорос;
- Вода;
- Соляная кислота в чистом виде.
Гальваническое меднение в домашних условиях
Приготовления раствора
Медный купорос
Делаем насыщенный раствор медного купороса, после чего нужно будет добавить 1/3 этого раствора в соляную кислоту. После приготовления раствора медного купороса его следует тщательно размешать, чтобы не было частиц. Далее нужно соляную кислоту тонкой струйкой добавить в этот раствор. Не следует забывать про технику безопасности и использовать перчатки и защитные очки. После того, как вы добавили в раствор соляную кислоту, его следует тщательно перемешать.
Итак, раствор готов и можно приступать к меднению в домашних условиях. Для этого нужно взять металлическую деталь, на которую вы собрались наносить слой меди и подготовить ее к работе. Подготовка включает в себя ее обработку наждачной бумагой. Данная процедура позволяет не только зачистить металлическую поверхность, но и обезжирить ее. Такая же процедура будет актуальна и для детали из латуни или свинца. После этого, покрытие нужно тщательно промыть в растворе кальцинированной соды. Это позволит более тщательно обезжирить материал.
Кальцинированная соды для обезжиривания материала
Далее поверхность нужно погрузить в раствор медного купороса и соляной кислоты. Следует обратить внимание на то, что первый слой меди является очень тонким и слабым, поэтому его желательно снять при помощи металлической щетки. После того, как вы это сделали, поверхность стали или свинца следует повторно промыть в растворе кальцинированной соды и опять погрузить в раствор для меднения. Данные манипуляции приведут к тому, что слой меди в домашних условиях на поверхности будет гораздо толще и гораздо крепче, поскольку его убрать можно будет с предмета, только используя наждачную бумагу, а не металлическую щетку как прошлый раз.
После того, как вы это сделали, поверхность стали или свинца следует повторно промыть в растворе кальцинированной соды и опять погрузить в раствор для меднения. Данные манипуляции приведут к тому, что слой меди в домашних условиях на поверхности будет гораздо толще и гораздо крепче, поскольку его убрать можно будет с предмета, только используя наждачную бумагу, а не металлическую щетку как прошлый раз.
Этот способ позволяет сделать очень качественное медное покрытие, которое можно снять только наждачкой. Для улучшения медного покрытия в домашних условиях следует деталь еще раз погрузить в раствор. Указанный способ отличается своей простотой и высокой эффективностью в том числе и для изделий из свинца.
Процедура меднения
Меднением принято называть процедуру гальванического нанесения меди, толщина слоя меди в таких случаях может составлять-от 300 мкм и больше. Меднение стали это один из наиболее важных процессов в гальванике, поскольку используется, как дополнительный процесс перед нанесением других металлов для хромирования, никелирования, покрытие серебром.
Слой меди прекрасно держится на стали и способен выравнивать различные дефекты на поверхности.
Для медных покрытий характерно высокое сцепление с другими поверхностями, изделиями из свинца особенно металлическими, а также высокая электропроводность и пластичность. Нанесенное недавно покрытие имеет ярко-розовый матовый или же блестящий цвет. Под воздействием влияний атмосферы медные покрытия могут окисляться, покрываться налетом окислов с различными пятнами радужного вида.
Сферы использования омеднения
Как правило, гальваническое омеднение может использоваться:
- В декоративных целях. С учетом огромной популярности в нынешнее время старинных изделий из меди. Существуют методы искусственного состаривания изделий из стали;
- В гальванопластике. Широко распространена в ювелирной сфере, среди сувенирной продукции, для изготовления барельефов и т.
 д;
д; - В технической отрасли. Меднение металла очень важно в электротехнической области. Низкая стоимость меднения по сравнению с покрытиями из золота или серебра позволяет снизить расходы на изготовление электродов, электротехнических шин, контактов и других элементов из сталии свинца.
Меднение происходит вместе с нанесением других гальванических покрытий
- Если нужно нанести многослойное защитно-декоративное покрытие на слой стали. В подавляющем большинстве случаев здесь медь используют вместе с никелем и хромом. Это позволяет улучшить сцепление с основным металлом и получить блестящее покрытие высокой прочности;
- Во избежание цементации участка. Меднение свинца позволит избежать появления углероживания на стальных участках. Для нанесения медного слоя используют только те участки, на которых будет проводиться обработка резанием;
- При выполнении реставрационных и восстановительных работ. Данный метод наиболее часто используется для восстановления хромированных частей автомобилей и мотоциклов. Для этих целей наносится довольно толстый слой меди, порядка 100-250 мкм и более того, что позволяет закрыть все дефекты и повреждения металла для нанесения последующих покрытий;
Разновидности меднения
- Используя погружение в электролит;
- Без погружения в электролит.
Первый способ предполагает обработку металлического изделия наждачной бумагой, щеткой и промывки водой. После чего обезжиривания в горячем содовом растворе с повторной промывкой. Далее в стеклянную емкость опускают на медных проволочках две медные пластины –аноды. Между пластинками на проволоке подвешивают деталь, после чего пускается ток.
Второй способ актуальный для изделий из стали, алюминия и цинка.
Домашнее омеднение
Данная процедура актуальна для различных случаев, поскольку нанесение слоя меди может использоваться для алюминиевых столовых приборов, сувениров, подсвечников и т. д. Неповторимый эффект оказывают изделия не из металла, на которые был нанесен слой меди.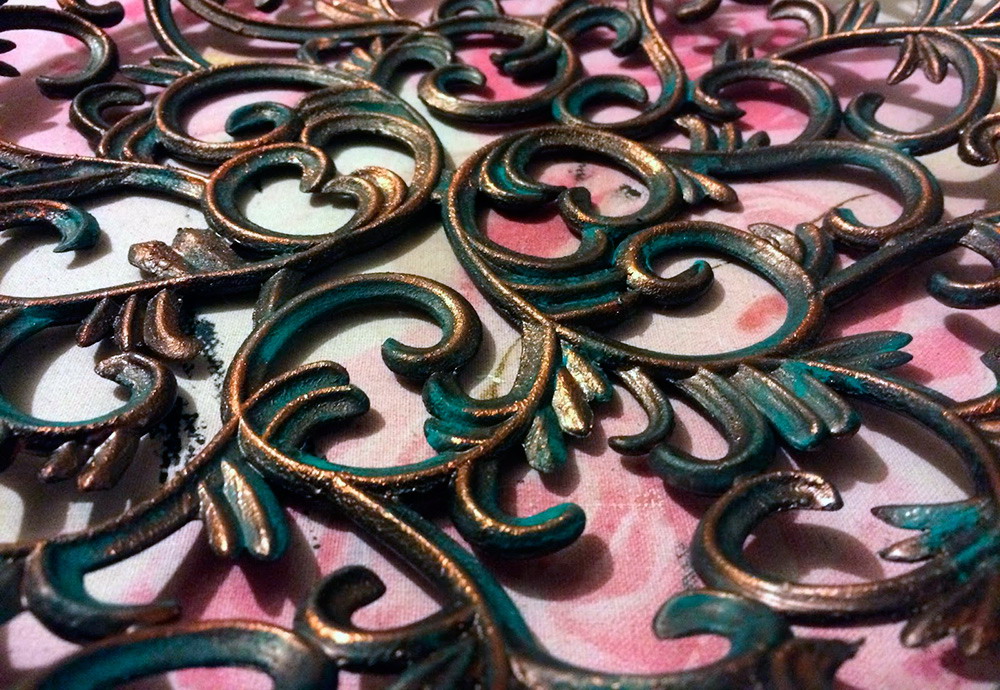 Это могут быть стебли растений, листья и др. Ввиду того, что в покрываемых предметах отсутствует токопроводящий слой, вместо него используется специальный электропроводный лак, который наносят на поверхности.
Это могут быть стебли растений, листья и др. Ввиду того, что в покрываемых предметах отсутствует токопроводящий слой, вместо него используется специальный электропроводный лак, который наносят на поверхности.
В состав лака входит ряд органических растворителей, пенкообразователей и тонкодисперсионный графитовый порошок, благодаря которому создается электропроводность. Лак наносят тонким слоем на сухую поверхность, и после высыхания через час можно приступать к омеднению. При желании можно меди придавать различные цветовые оттенки, используя для этого специальные способы. Высокое качество и уникальность таких изделий вполне заслуженно приравнивается к настоящим ювелирным украшениям.
Видео: Меднение в домашних условиях
Гальваническое меднение стали, алюминия, металла, чугуна; покрытие медью по выгодной цене
Компания «Гальваник Про» оперативно выполнит меднение изделий любой сложности из стали, алюминия, цинка, других материалов. Характеристики готовой продукции соответствуют заданным техническим условиям и требованиям ГОСТ.
Чаще всего меднение применяется в целях создания подслоя перед нанесением других покрытий для повышения их адгезии к основе и улучшения коррозионной стойкости. Поверхность металла подвергается тщательному обезжириванию, очистке и травлению для удаления поврежденного слоя. В результате прочность сцепления между металлом основы и электроосажденной медью сравнима с прочностью соединения атомов в самом металле.
При нанесении суммарного покрытия, состоящего из меди, никеля и хрома, медь уменьшает пористость поверхности, экономит более дорогие материалы и упрощает механическую обработку деталей.
Другие задачи, которые решает меднение:
- защита поверхности стали от цементации (науглероживания)
- образование искробезопасного покрытия
- увеличение тепло- и электропроводности изделий
- повышение декоративности элементов интерьера, ландшафта, сувенирной продукции, мебельной фурнитуры, сантехнических приборов
Перед началом работы опытный специалист подбирает конкретные технологические приемы для получения качественного, равномерного и долговечного медного слоя. В зависимости от требований заказчика используются блестящие, нейтральные или матовые электролиты.
В зависимости от требований заказчика используются блестящие, нейтральные или матовые электролиты.
Компания «Гальваник Про» гарантирует:
- Высокое качество меднения. Длительный эксплуатационный срок покрытия достигается за счет грамотной подготовки поверхности и постоянного контроля за процессом гальванизации.
- Отличный сервис. Вы можете получить у нас профессиональные рекомендации по подбору гальванического покрытия исходя из типа изделия и условий его эксплуатации. Найдем оптимальный вариант, который подойдет вам по функциональным свойствам и цене.
- Соблюдение сроков. Четкое планирование производства позволяет нам избежать задержек и вовремя отгрузить готовую продукцию.
Стоимость меднения зависит от конфигурации детали, площади поверхности, толщины слоя и необходимости в дополнительной обработке. Для предварительного расчета цены и определения срока исполнения заказа свяжитесь с нашими технологами по телефону 8 (985) 255-94-94 или отправьте заявку посредством формы обратной связи.
Медь в качестве основного материала | Покрытие медных деталей
Покрытие на медь
Медь — мягкий, пластичный металл, который используется во многих промышленных процессах и приложениях. Превосходные тепловые свойства и высокая электропроводность меди делают ее лучшим выбором для производства таких продуктов, как провода и кабели, интегральные схемы и печатные платы, проводники, электродвигатели, строительные материалы, трубопроводы и многие другие изделия.
Медь доступна в больших количествах, и это также один из немногих металлов, которые можно найти в пригодной для использования форме — ее не нужно извлекать из руды.Эти характеристики делают использование меди в производстве очень рентабельным.
Легирование меди другими металлами
Чистая медь (UNS C11000 — чистота меди 99,9%) часто используется в производстве электроники. Однако производство медных сплавов путем объединения их с другими металлами является обычной практикой в других отраслях промышленности. Создание сплава с одним или несколькими металлами улучшит характеристики меди, а также других материалов, и сделает ее более пригодной для самых разных промышленных процессов.Также легче производить сплавы с медью, чем из большинства металлических материалов. Примеры сотен медных сплавов включают:
Однако производство медных сплавов путем объединения их с другими металлами является обычной практикой в других отраслях промышленности. Создание сплава с одним или несколькими металлами улучшит характеристики меди, а также других материалов, и сделает ее более пригодной для самых разных промышленных процессов.Также легче производить сплавы с медью, чем из большинства металлических материалов. Примеры сотен медных сплавов включают:
- Латунь: При объединении меди с цинком образуется латунь — материал желтоватого цвета, известный своим сходством с золотом. Хотя латунь часто используется в декоративных целях, изменение количества меди и цинка привнесет ценные производственные свойства, такие как твердость, электрическая и теплопроводность и коррозионная стойкость.
- Медно-никелевый сплав: Добавление никеля в медь увеличивает ее прочность и устойчивость к коррозии.Общие промышленные применения включают морское загрязнение и биообрастание.
- Бериллий-медь: Бериллий повышает твердость меди. Бериллиево-медный сплав проявляет механические свойства, аналогичные высокопрочным сталям. Бериллий также не образует оксидов до достижения чрезвычайно высоких температур.
- Бронза: Бронза состоит из комбинации меди и других металлов, таких как олово, алюминий и кремний. Фосфорная бронза — это медно-оловянный сплав, известный своей прочностью, хорошей защитой от износа и отличной коррозионной стойкостью.
- Мельхиор: Мельхиор — это медно-никелевый сплав, который также содержит такие металлы, как марганец и железо, для дополнительной прочности. Купроникель обеспечивает превосходную стойкость к коррозии, вызываемой морской водой, что делает его популярным для морских применений.
Покрытие медными сплавами
Хотя легирование меди другими металлами обеспечивает множество полезных свойств для производственных целей, иногда необходимо улучшить эти характеристики и / или ввести новые свойства. Для достижения этих целей существует несколько проверенных временем методов обработки металла:
Для достижения этих целей существует несколько проверенных временем методов обработки металла:
- Гальваника: Гальваника наносит дополнительное покрытие на поверхность подложки из медного сплава. Заготовка погружается в раствор электролита, содержащий растворенные ионы другого металла. Подача постоянного тока стимулирует реакцию, которая покрывает подложку металлом в результате электроосаждения.
- Гальваническое покрытие: Гальваническое покрытие также покрывает медный сплав другим металлическим материалом.Однако этот метод не требует электрического тока. Напротив, осаждение происходит в результате автокаталитической реакции, которая происходит между заготовкой и жидким раствором для гальваники.
Способы нанесения покрытия на медь и медные сплавы
Гальваника меди и медных сплавов — обычная практика при производстве деталей для таких отраслей, как аэрокосмическая, автомобильная, оборонная и электронная. Типичные металлы, используемые для меднения, включают:
- Олово: Покрытие из олова повысит рабочую температуру медной подложки и улучшит ее паяемость.Олово также дешевле, чем многие другие металлы, что делает его подходящим способом гальваники меди для экономичных компаний. Лужение следует применять только на основных материалах, которые не подвергаются высокотемпературной обработке после нанесения покрытия.
- Серебро: Посеребрение меди увеличивает рабочую температуру проводов из медного сплава. Серебро также обеспечивает превосходную паяемость и отличную электропроводность. Когда серебро используется для покрытия медного проводника, оно улучшает возможности передачи высоких частот.
- Никель: Гальваническое никелевое покрытие повышает коррозионную стойкость медной подложки и повышает рабочую температуру. Однако из-за твердости никеля никелированные проводники, как правило, демонстрируют большую вариабельность заделки обжима, чем другие металлические материалы.

- Многослойное покрытие: Некоторые процессы гальваники меди предполагают последовательное осаждение нескольких металлов на подложку. Это уменьшит реакцию между основным металлом и поверхностью, сохраняя при этом полезные свойства покрытия поверхности.
- Никель, полученный методом химического восстановления: Никель, нанесенный химическим способом, часто наносится на медные электронные компоненты на заключительном этапе производственного процесса. Это включает нанесение химического никеля с иммерсионным золотом на следы меди.
SPC предлагает комплекс услуг по гальванике меди
Независимо от того, какой тип медного сплава вы используете в производственных процессах, SPC может реализовать процесс высококачественного меднения, который улучшит характеристики, долговечность и внешний вид ваших деталей.Обладая более чем 90-летним опытом в области обработки металлов, вы можете рассчитывать на то, что мы порекомендуем правильный процесс для ваших приложений. Свяжитесь с нами для получения бесплатного предложения по медному покрытию!
Дополнительные ресурсы:
Как работает гальваника — Объясни, что материал
Криса Вудфорда. Последнее изменение: 28 июля 2020 г.
Не существует такой вещи, как алхимия — волшебным образом превращающая обычные химические элементы в редкие и ценные — но гальваника, возможно, является следующим лучшим занятием.Идея состоит в том, чтобы использовать электричество для покрытия относительно приземленных металл, например медь, с тонким слоем другого, более ценного металл, например золото или серебро. Гальваника имеет много других применений, помимо того, что дешевые металлы выглядят дорогими. Мы можем использовать это, чтобы сделать устойчивые к ржавчине вещи, например, для производства различных полезных сплавы, такие как латунь и бронза, и даже чтобы пластик был похож на металл. Как работает этот удивительный процесс? Давайте посмотрим внимательнее!
Фото: Гальваника в действии — выставка в Think Tank (музей науки в Бирмингеме, Англия). Эти две вилки являются электродами, и синий раствор (сульфат меди) используется для медного покрытия одной из них.
Эти две вилки являются электродами, и синий раствор (сульфат меди) используется для медного покрытия одной из них.
Что такое гальваника?
Фото: Позолоченное: Когда астронавт Эд Уайт совершил первый выход в открытый космос в 1965 году, на его шлеме был позолоченный козырек, защищавший глаза от солнечного излучения. Фото любезно предоставлено НАСА в палате общин.
Гальваника включает пропускание электрического тока через раствор, называемый электролит.Это делается путем погружения двух клемм, называемых электроды в электролит и подключив их к цепь с аккумулятором или другим источником питания. Электроды и электролит состоит из тщательно подобранных элементов или соединений. Когда электричество проходит через цепь, которую они образуют, электролит расщепляется, и некоторые из атомов металла, которые он содержит, наносится тонким слоем поверх одного из электродов — он становится гальваническим. Все виды металлов могут быть покрытым таким образом, в том числе золотом, серебром, олово, цинк, медь, кадмий, хром, никель, платина и свинец.
Гальваника очень похожа на электролиз. (используя электричество для расщепления химического раствора), что является обратным процессу, при котором батареи производят электрические токи. Все это примеры электрохимия: химические реакции, вызванные или производящие электричество, которое дает полезные в научном или промышленном отношении конечные продукты.
Фото: Серебряные столовые приборы дороги и тускнеют; нержавеющая сталь с хромовым покрытием является хорошей заменой для многих людей.Несмотря на то, что он устойчив к ржавчине и долговечен, покрытие со временем изнашивается, как вы можете видеть в коричневатой области в центре этого пирогового сервера. Маркировка «EPNS» на столовых приборах является окончательным знак покрытия: это гальванический нейзильбер.
Как работает гальваника?
Во-первых, вы должны выбрать правильные электроды и электролит, определив
химическая реакция или реакции, которые должны произойти, когда электрический
ток включен. Атомы металла, покрывающие ваш объект, исходят из
электролит, поэтому, если вы хотите что-то медить, вам понадобится электролит
изготовлен из раствора соли меди, а для золочения понадобится
электролит на основе золота и так далее.
Атомы металла, покрывающие ваш объект, исходят из
электролит, поэтому, если вы хотите что-то медить, вам понадобится электролит
изготовлен из раствора соли меди, а для золочения понадобится
электролит на основе золота и так далее.
Затем вы должны убедиться, что электрод, который вы хотите наклеить, полностью чистый. В противном случае, когда атомы металла из электролита осаждаются на это, они не сформируют хорошую связь, и они могут просто стереться снова. Как правило, чистка выполняется путем погружения электрода в прочный кислотным или щелочным раствором или (кратковременно) подключив гальваника в обратном направлении. Если электрод действительно чистый, атомы металла покрытия эффективно связываются с ним, соединяясь очень сильно на внешние края его кристаллической структуры.
Изображение: Медное покрытие латуни: Вам понадобится медный электрод (серый, слева), латунный электрод (желтый, правый) и немного раствора сульфата меди (синий). Латунный электрод становится отрицательно заряженным и притягивает из раствора положительно заряженные ионы меди, которые прилипают к нему и образуют внешнее покрытие медной пластины.
Теперь мы готовы к основной части гальваники. Нам нужны два электрода из
различные проводящие материалы, электролит и электричество
поставлять.Обычно один из электродов делается из металла, который мы
пытаясь пластину, а электролит представляет собой раствор соли
тот же металл. Так, например, если мы покрываем медью латунь, мы
нужен медный электрод, латунный электрод и раствор
соединение на основе меди, такое как раствор сульфата меди. Металлы, такие как
золото и серебро не растворяются легко, поэтому их нужно превращать в
растворы с использованием сильнодействующих и опасно неприятных химикатов на основе цианидов.
Электрод, на который будет наноситься покрытие, обычно изготавливается из более дешевой
металл или неметалл, покрытый проводящим материалом, таким как
графит.В любом случае он должен проводить электричество или не проводить электричество. ток будет течь, и никакого покрытия не произойдет.
ток будет течь, и никакого покрытия не произойдет.
Мы окунаем два электрода в раствор и соединяем их в цепь так, чтобы медь становится положительным электродом (или анодом), а латунь становится отрицательным электродом (или катодом). Когда мы включаем мощности раствор сульфата меди расщепляется на ионы (атомы с мало или слишком много электронов). Ионы меди (которые положительно заряжены) притягиваются к отрицательно заряженному латунному электроду и медленно нанесите на него, производя тонкий позже медной пластины.Между тем, сульфат-ионы (которые отрицательно заряжены) приходят к положительно заряженному медному аноду, высвобождая электроны которые движутся через батарею к отрицательному латунному электроду.
Гальваническим атомам требуется время, чтобы накапливаться на поверхности отрицательного электрода. Сколько именно времени зависит от силы электрического тока у вас использование и концентрация электролита. Увеличение любого из это увеличивает скорость, с которой ионы и электроны движутся через схема и скорость процесса нанесения покрытия.Пока по мере того как ионы и электроны продолжают двигаться, ток продолжает течь, и процесс нанесения покрытия продолжается.
Можно ли гальванизировать пластмассы?
Фото: Пластик с покрытием часто используется для деталей, которым требуется блестящая отделка металла без его прочности и тяжести, и вот три примера из моего собственного дома. Вверху: переключатель, стрелки и безель (рамка циферблата) этого будильника выглядят блестящими и металлическими, но на самом деле они пластиковые. В центре: детали водопровода, которые не должны быть прочными, часто изготавливаются из пластика с покрытием, поэтому они остаются прохладными на ощупь и гармонируют с металлическими трубами.Регулятор температуры на этом душе (справа, с красной кнопкой) сделан из пластика, но похож на основные металлические компоненты слева. Внизу: компьютерный USB-микрофон имеет глянцевую поверхность, чтобы он выглядел дорогим и высококачественным.
Недорогой, легко поддающийся формованию, легкий и одноразовый, пластмассы быстро стали наиболее распространенными и гибкими материалами в 20 веке. Но для многих это не только преимущество, но и недостаток: пластик дешевый и дешевый — и именно так они выглядят.Одно из решений — покрыть дешевый пластик тонким слоем металла, чтобы придать ему все преимущества пластика с привлекательной блестящей отделкой. металл. Таким способом можно покрыть множество различных пластиков, в том числе АБС-пластик, фенольные пластики, карбамидоформальдегид, нейлон и т. Д. и поликарбонат. Вы часто найдете детали на автомобилях, сантехнике, бытовой и электрической арматуре, которые выглядят металлическими, но на самом деле являются пластиковыми покрытиями. Они легче, дешевле, устойчивы к ржавчине и не требуют полировки после нанесения покрытия.
Как на пластмассы наносят гальваническое покрытие?
«… мой приятель … сказал мне, что у него есть процесс металлизации пластмасс. Я сказал, что это было невозможно, потому что нет проводимости; нельзя прикрепить провод. Но он сказал, что может наклеить металлическими пластинами все, что угодно … «
Вы, конечно, шутите, мистер Фейнман! Ричард Фейнман
Если вы что-нибудь знаете о пластике, вы сразу заметите очевидную проблему: пластик обычно не проводит электричество. Теоретически это должно полностью исключить гальваническое покрытие; на практике это просто означает, что мы должны дополнительно обработать наш пластик, чтобы он стал электропроводящим, прежде чем мы начнем.Есть несколько этапов. Во-первых, пластик необходимо тщательно очистить от таких вещей, как пыль, грязь, жир и следы с поверхности. Затем его протравливают кислотой и обрабатывают катализатором (ускорителем химической реакции), чтобы обеспечить прилипание покрытия к его поверхности. Затем его окунают в ванну из меди или никеля (медь более распространена), чтобы получить очень тонкое покрытие из электропроводящего металла (толщиной менее микрона, 1 мкм или одной тысячной миллиметра). Как только это будет сделано, на него можно будет нанести гальваническое покрытие, как на металл. В зависимости от того, сколько износа должна выдержать металлическая деталь, толщина покрытия может быть от 10 до 30 микрон.
Как только это будет сделано, на него можно будет нанести гальваническое покрытие, как на металл. В зависимости от того, сколько износа должна выдержать металлическая деталь, толщина покрытия может быть от 10 до 30 микрон.
Зачем нужна гальваника?
Фото: Это автомобильное колесо изготовлено из металлического алюминия, покрытого никель в более экологически чистом процессе, разработанном Metal Arts Company, Inc. В процессе Microsmooth ™ используется примерно на 30 процентов меньше электроэнергии, почти на 60 процентов меньше природного газа и вдвое меньше воды, чем требуется для традиционных процессов нанесения покрытий.Фото: Metal Arts Company, Inc. любезно предоставлено Министерством энергетики США (DOE).
Гальваника обычно выполняется по двум совершенно разным причинам: украшение и защита.
Металлы, такие как золото и серебро, покрываются для украшения: дешевле иметь золото или
посеребренные украшения, чем цельные изделия из этих тяжелых,
дорогие, ценные вещества. Потому что разные металлы разных цветов,
гальваника может использоваться для изготовления таких вещей, как кольца, цепочки, значки, медали и т. д.
широкий выбор привлекательной декоративной отделки,
включая блестящие, матовые и старинные варианты золота, серебра, меди, никеля и бронзы.Металлы, такие как олово и цинк (которые не особенно привлекательны на вид), покрываются гальваническим покрытием,
защитный внешний позже. Например, пищевые контейнеры
часто покрывают оловом, чтобы сделать их устойчивыми к коррозии, в то время как многие
предметы быта из железа покрыты
цинк (в процессе, называемом гальванизацией) по той же причине.
Некоторые формы гальваники являются как защитными, так и декоративными. Крылья автомобилей и «отделка», например, когда-то
широко изготовлен из прочной стали с покрытием
с хромом, чтобы сделать их привлекательно блестящими и
устойчивы к ржавчине (теперь более вероятны недорогие и естественно устойчивые к коррозии пластмассы
для использования на автомобилях). Сплавы, такие как латунь и бронза, также могут быть покрыты
обеспечение содержания в электролите солей всех металлов, которые
должен присутствовать в сплаве. Гальваника также используется для
изготовление дубликатов печатных форм в процессе, называемом
электротипирование и гальванопластика (альтернатива
литье изделий из расплавленных металлов).
Сплавы, такие как латунь и бронза, также могут быть покрыты
обеспечение содержания в электролите солей всех металлов, которые
должен присутствовать в сплаве. Гальваника также используется для
изготовление дубликатов печатных форм в процессе, называемом
электротипирование и гальванопластика (альтернатива
литье изделий из расплавленных металлов).
Насколько толсто гальваническое покрытие?
Независимо от того, покрывают ли вещи покрытие для украшения или защиты, толщина слоя покрытия является еще одним важным фактором. рассмотрение.Очевидно, что чем толще покрытие, тем дольше оно прослужит и тем большую защиту будет давать, но даже самая толстая обшивка намного тоньше, чем можно было ожидать. Типичная толщина плакированного металла варьируется от примерно От 0,5 микрон (0,5 миллионных долей метра или 0,0005 миллиметра) до примерно 20 микрон (20 миллионных долей метра или 0,02 миллиметра) — так это очень тонкий. (Чтобы дать вам некоторое представление, алюминиевая кухонная фольга находится примерно в середине этого диапазона, с самая толстая и прочная фольга — около 10–20 микрон.) Что-то вроде позолоченного корпуса часов будет иметь покрытие в 20 микрон, которое может легко выдержать повседневные грубые дела. и кувыркается несколько десятилетий.
Если вам понравилась эта статья …
… вам могут понравиться мои книги. Мой последний Breathess: почему загрязнение воздуха имеет значение и как оно влияет на вас.
Узнать больше
На сайте
Мероприятия
Гальваника — это то, с чем можно легко поэкспериментировать в школе или (с помощью взрослого) дома.Вот несколько сайтов, которые вы можете безопасно исследовать:
Видео
- Гальваника — как это делается: четкое введение в теорию и практику гальваники и огромное количество повседневных вещей, для которых она используется. Также описывается, как на пластмассы можно наносить гальваническое покрытие и почему гальванику часто необходимо наносить несколькими отдельными слоями или «слоями».

- Гальваника четверти: ясно и просто объяснено в этом коротком видео от учителя химии мистера Кента.
Книги
Для читателей постарше
- Гальваника: Инженерное руководство Лоуренса Дж. Дерни (ред.). Springer, 2014. Еще один подробный справочник, в основном предназначенный для людей, работающих в индустрии обработки металлов.
- Гальваника: основные принципы, процессы и практика Нассера Канани. Elsevier, 2004. Подробное введение для студентов-химиков, а также производителей.
- Современное гальваническое покрытие Мордехая Шлезингера, Милана Пауновича (ред.).Wiley, 2011. Огромное и подробное руководство с главами по гальванике всех распространенных металлов, включая медь, никель, золото и олово; плюс освещение электроосаждения, полупроводников, органических пленок и многих других тем.
- Вы, конечно, шутите, мистер Фейнман! Ричард П. Фейнман. Винтаж, 1992. Глава под названием «Главный химик-исследователь корпорации MetaPlast Corporation» (стр. 41 моего издания) представляет собой короткий, но забавный анекдот о гальванических пластиках, первым из которых, как оказалось, был Фейнман.
Для младших читателей
Это лучше всего для детей в возрасте 9–12 лет, но эксперименты можно адаптировать для детей старшего и младшего возраста.
- Химия для каждого ребенка: 101 простой эксперимент, который действительно работает, Дженис ВанКлив. Jossey-Bass, 2010. Очень хорошее практическое введение в химию (с добавлением немного физики и биологии, если это необходимо). Первоначально опубликовано в 1989 году, но не менее актуально сегодня. Мероприятие 43 (Зеленые пенни) — это пример металлизации.
- Пошаговые научные эксперименты в химии Дженис ВанКлив. Розен, 2013. Более новая и короткая подборка того же автора.
- Роберт Уинстон «Это элементарно». ДК, 2007/2016. Общее введение в химию для детей в возрасте 8–10 лет, посвященное элементам.
Статьи
Современная обшивка
Исторические статьи из архивов
Патенты
Для получения более подробной технической информации их стоит просмотреть:
- Патент США 6527920: устройство для гальваники меди, автор Стивен Т.
 Майер и др., Novellus Systems, Inc., 4 марта 2003 г. Подробное описание видов гальванических процессов, используемых при создании интегральных схем.
Майер и др., Novellus Systems, Inc., 4 марта 2003 г. Подробное описание видов гальванических процессов, используемых при создании интегральных схем. - Патент США 4 039 714: процесс гальваники меди, Ютака Окинака, AT&T Bell Laboratories. 4 сентября 1984 г. Описывается типичная современная ванна для меднения.
- Патент США 4 039 714: Предварительная обработка пластмасс для металлизации, авторы Иржи Рубаль и Иоахим Корпиун. 2 августа 1977 года. Здесь подробно рассказывается о том, как поверхность пластика может быть подготовлена к гальванике.
Что вы должны знать о медном покрытии — Услуги по нанесению золотого покрытия
Археологические раскопки показали, что медь была частью самых ранних цивилизаций. На протяжении всего времени он использовался для самых разных целей, от ювелирных изделий до скульптур и рабочих инструментов и столовых приборов.
(Pixabay / sferrario1968)
Медь считается одним из первых металлов, обнаруженных и использованных людьми, и неудивительно, что люди восприняли эту стихию как блеск.Медь податлива, мягка и гибка, но прочна. Эти качества делают медь чрезвычайно доступным и полезным материалом для многих применений.
Медь для гальваники
Сегодня медь широко используется в гальванике, что влечет за собой использование электричества для нанесения очень тонкого слоя меди на другую металлическую или пластиковую поверхность. Гальваника медью — это метод, широко используемый в промышленности, в основном для защиты других металлов от коррозии. Его часто используют в качестве подслоя для дальнейшего гальванического покрытия из-за его гладкого и равномерного покрытия.Гальваника меди также используется перед пайкой, особенно в электронной и аэрокосмической промышленности.
Открытие меди в гальванике помогло промышленным предприятиям продвинуться вперед в их повседневных операциях. Трудно представить мир без машин и предметов, покрытых медью.
Давайте посмотрим на некоторые из различных применений меднения:
- Поскольку медь является отличным проводником, она хорошо работает в сочетании с радиочастотными и электромагнитными помехами.
- Медь часто используется в качестве подложки для серебряных или никелевых покрытий, поскольку она помогает им склеивать лучше, чем в противном случае.
- Медь используется в медицине, потому что она очень устойчива к бактериям.
- Медь используется для сглаживания дефектов поверхности и обеспечения желаемой отделки алюминиевых дисков.
- Гальваника меди может вдохнуть новую жизнь в изношенные кастрюли и сковороды.
- Сегодня монеты изготавливаются из стали с добавлением слоя меди, потому что пластинчатую сталь проще и дешевле, чем изготовление твердых медных монет.
- Наконец, конечно, медь может улучшить внешний вид металлических и пластиковых предметов.
Медь реагирует с другими минералами
Медь является очень подходящим элементом для гальваники во многих областях, но также существуют ограничения на ее использование из-за некоторых специфических свойств металла. Медь, как активный металл, не может быть использована для прямого покрытия железом без первоначального нанесения никелевого основного покрытия. Когда базовое покрытие высыхает, добавляется медное покрытие, которое делает металл прочнее и подготавливает его для различных целей.
Кроме того, может потребоваться использование раствора цианида в сочетании с раствором меди для обеспечения максимальной адгезии. Однако цианид, будучи высокотоксичным, требует значительной осторожности во время процесса нанесения покрытия. Медь также имеет естественный тусклый цвет, а это означает, что для создания этой фирменной яркой отделки требуются дополнительные действия.
Хромирование и никелирование меди
Медь — в высшей степени универсальный металл, который полезен для различных отраслей промышленности благодаря эффективной проводимости и ковкости.
Хотя ее преимущества обычно перевешивают ее недостатки, медь все же подвержена различным проблемам, в первую очередь коррозии и снижению прочности. Вы также можете оказаться в ситуациях, требующих улучшения природных свойств меди.
Вы можете создать более округлый металл с помощью услуг по нанесению покрытий, и специалисты Hard Chrome выполнят ваши требования. Наша компания имеет сертификат ISO, который тщательно анализирует ваши потребности и решает их, предлагая первоклассное обслуживание в короткие сроки.
Можно ли хромировать медь?
Жесткое хромирование меди может показаться нетрадиционным, но оно оказалось весьма полезным в различных отраслях промышленности.
Процесс аналогичен процессу хромирования стали. Мы тщательно очистим медь от грязи и сажи, а затем активируем ее кислотным рассолом, прежде чем нанести никель. Затем мы окунем его в электрохимическую ванну с хромом, которую мы будем постепенно стимулировать с увеличением электрического тока, чтобы образовался тонкий слой хрома на меди.
Преимущества хромирования меди
Медь подвергается естественной коррозии, образуя патину или зеленоватое оксидное покрытие снаружи. Многослойное покрытие хромом может решить эти проблемы, так как оно значительно увеличивает защиту от коррозии благодаря ровному слою и естественной устойчивости ко многим элементам.
Он также увеличивает твердость, что помогает смягчить естественную мягкость меди. Вы получите отчетливый блестящий блеск, который облегчает обнаружение деталей и делает их более эстетичными.
Каковы общие области применения хромирования меди?
Вы можете нанести хромирование на медные инструменты, испарители льдогенераторов, водопроводные трубы и фитинги и даже на произведения искусства.
Можно ли никелировать медь?
В этом процессе используются химические реагенты в водном растворе для ускорения осаждения, что отличается от гальванического покрытия наших хромовых погружений.
Для химического никелирования меди требуется особая обработка по сравнению с другими металлами.Поскольку медь не является каталитической в отношении этого процесса, для нее нужен своего рода скачок. Мы можем облегчить процесс, подав электрический ток на несколько секунд перед тем, как начать замачивание.
Мы также можем применить общий удар никеля в отдельном резервуаре, так как он будет способствовать развитию каталитических центров.
Преимущества химического никелирования меди
Хотя его преимущества в чем-то аналогичны нашему хромированию, этот процесс сделает даже больше, чем значительно повысит коррозионную стойкость и прочность.
Покрытие медью также увеличивает общую электрическую проводимость, поскольку никель также является хорошим проводником. Никель также повышает рабочую температуру металла, что делает его более идеальным для тяжелых условий эксплуатации.
Каковы общие области применения химического никелирования меди?
Когда вы увеличиваете электрическую проводимость меди, вы делаете ее еще лучшим материалом для электрических компонентов. Поскольку никелирование увеличивает рабочую температуру металла, никелированная медь также идеально подходит для применений с высокими тепловыми требованиями.
Вы можете интегрировать химическое никелирование в провода и кабели, интегральные схемы и печатные платы, проводники, детали электродвигателей, трубопроводы и другие подобные предметы.
Чтобы узнать больше о покрытии меди, заполните нашу контактную форму или позвоните нам по телефону 717-764-5171, чтобы запросить смету.
Precious Plate — Точечное покрытие, выборочное покрытие, гальваническое покрытие> Возможности нанесения покрытия> Никель и медь
Обычно никелирование и меднение применяются в качестве грунтовки для золота, палладия, серебра и олова.Эти подкладки вносят свой вклад в характеристики всего покрытия, улучшая коррозионную стойкость, износостойкость и способность к пайке, а также ограничивая потенциальную диффузию элементов из основного металла в поверхностный слой во время тепловых колебаний ниже по потоку.
Precious Plate понимает важность качественного покрытия
Мы стараемся обеспечить исключительно чистые грунтовки из никеля и меди. Невыполнение этого требования может вызвать серьезные проблемы с долговременной производительностью продукта . Следовательно, Precious Plate обеспечивает непрерывную фильтрацию, очистку и анализ всех процессов гальваники меди и никеля, чтобы гарантировать отсутствие загрязнений.
Почему стоит рассмотреть возможность нанесения гальванического покрытия на никель?
Precious Plate покрывает большинство деталей никелем. Никелирование обеспечивает отличную коррозионную и износостойкость и действует как исключительный барьер, предотвращающий миграцию компонентов основного материала в золото, палладий или другие металлы.Никелевое покрытие или предварительное покрытие также является ключевым шагом для предотвращения роста нитей олова.
Преимущества никелирования
- Никель обеспечивает защиту от коррозии
- Никель износостойкий
- Никель обеспечивает хороший барьер между основным материалом и драгоценными металлами
- Никель помогает уменьшить рост усов олова
Медное гальваническое покрытие обеспечивает исключительную грунтовку
Медь — еще одна широко используемая подкладка.Медь хорошо прилипает к множеству различных основных материалов, а также к металлу с последующим покрытием. Медь также является отличным проводником тепла и электричества, что делает ее популярной для многих инженерных приложений.
Преимущества гальваники меди
- Медь отлично проводит тепло и электричество
- Медь обеспечивает хороший барьер между основным материалом и последующими отложениями.
- Медь хорошо сцепляется со многими другими металлами
- Медь пластичная
Свяжитесь с нами, чтобы обсудить ваш индивидуальный проект промышленного никелирования или меднения сегодня!
Медное покрытие | Спектрметаллфиниш
Медь для гальваники — это металл, на который чаще всего наносят покрытие, кроме никелирования. Причина популярности меднения заключается в том, что меднение или, что обычно называют медным покрытием, является отличным грунтовочным покрытием для последующего нанесения металлического покрытия. Медное покрытие служит хорошим металлом для покрытия дефектов подложки, таких как осколки, ямки и другие дефекты, вызванные литьем под давлением свинцом или цинком. полировка или полировка меди, которые очень легко сделать, улучшают ее способность служить отличным субстратом. Медь может обеспечить легкий, ровный и светлый субстрат.Кроме того, медь относится к числу менее дорогих металлов, и ее предложение стабильно. Большее выравнивание или толщину покрытия может быть получено путем меднения за счет гальванического покрытия металла, чем для любого другого металла с гальваническим покрытием.
Причина популярности меднения заключается в том, что меднение или, что обычно называют медным покрытием, является отличным грунтовочным покрытием для последующего нанесения металлического покрытия. Медное покрытие служит хорошим металлом для покрытия дефектов подложки, таких как осколки, ямки и другие дефекты, вызванные литьем под давлением свинцом или цинком. полировка или полировка меди, которые очень легко сделать, улучшают ее способность служить отличным субстратом. Медь может обеспечить легкий, ровный и светлый субстрат.Кроме того, медь относится к числу менее дорогих металлов, и ее предложение стабильно. Большее выравнивание или толщину покрытия может быть получено путем меднения за счет гальванического покрытия металла, чем для любого другого металла с гальваническим покрытием.
Медное покрытие не только служит базовым слоем для других процессов гальваники, но также обычно используется в качестве отдельного металлического покрытия. Яркое или декоративное медное покрытие обеспечивает коррозионно-стойкую поверхность для таких применений, как покрытие стальной проволоки и литье под давлением цинка.Он также часто используется в электронной промышленности, чтобы сделать непроводящие проводники проводящими, а также на печатных платах и других электронных устройствах.
Spectrum Metal Finishing предлагает услуги по медному покрытию как стоек, так и цилиндров различных размеров и спецификаций. Spectrum использует кислотную медную ванну, которая обеспечивает блестящее или декоративное покрытие медью поверх блестящего никелевого покрытия. Кроме того, Spectrum также использует ванну для меднения, которая предназначена для обеспечения основного слоя перед добавлением дополнительных слоев золотого покрытия, серебряного покрытия, никелирования, черного никелирования, латунного покрытия, химического никелирования и нашей экологически чистой хромовой альтернативы. .
Чтобы получить дополнительную информацию об услугах Spectrum по медному покрытию, отправьте детали вашего запроса, используя эту форму. Пожалуйста, включите подробную информацию о вашем продукте, такую как размер и форма продукта, применение продукта, требуемая отделка, подложка или основной материал, из которого изготовлен продукт, годовое количество и любую другую информацию, которая поможет нам предоставить точную цитату. На все запросы будет дан ответ в течение 24 часов с момента получения.
Пожалуйста, включите подробную информацию о вашем продукте, такую как размер и форма продукта, применение продукта, требуемая отделка, подложка или основной материал, из которого изготовлен продукт, годовое количество и любую другую информацию, которая поможет нам предоставить точную цитату. На все запросы будет дан ответ в течение 24 часов с момента получения.
Услуги по медному покрытию | American Plating Company
Преимущества и использование медного покрытия
Меднение — это процесс нанесения медного покрытия на металлическую поверхность.Кроме того, медь имеет красновато-оранжевый оттенок и от природы мягкая и податливая в умеренном климате. В металлообрабатывающей промышленности меднение является популярным выбором среди коммерческих покрытий. Фактически, после никеля, медь является второй наиболее часто используемой отделкой в индустрии металлических покрытий.
5 главных преимуществ меднения:
В целом, широкое использование меди обусловлено многими благоприятными свойствами металла, в том числе:
1. Электропроводность: Медь является хорошим проводником электричества.Поэтому он обеспечивает отличную электропроводность электрических компонентов. В результате в электротехнической и электронной промышленности проводимость является ключевым фактором.
2. Пластичность : Поскольку медь является мягким металлом, ее лучше всего использовать для металлических предметов, которым требуется небольшая гибкость. При правильном покрытии медь не будет расслаиваться и сохранять хорошую адгезию даже в условиях изгиба металла.
Нанесение медного покрытия на стальные детали с помощью электрического тока, дополнительно с использованием трех различных типов химических ванн: ( 1) Щелочная, ( 2) Кислотная и ( 3) Слабощелочная обработка. укрепляет медь в стали. .
3.


 д;
д;

 Майер и др., Novellus Systems, Inc., 4 марта 2003 г. Подробное описание видов гальванических процессов, используемых при создании интегральных схем.
Майер и др., Novellus Systems, Inc., 4 марта 2003 г. Подробное описание видов гальванических процессов, используемых при создании интегральных схем.